“만약 지구가 태양에 조금 더 가까워서 기온이 물의 끓는 점보다 높았다면 대부분의 액체들, 심지어 일부 금속들도 기체가 되어 대기를 형성했을 것이다. 반면에 지구가 목성이나 토성처럼 조금 더 추운 곳에 있었다면, 강과 바다의 물 대신 지구에는 얼음산이 존재했을 것이다. 공기는, 전부는 아니라 하더라도 적어도 공기 중 일부는, 눈에 안 보이는 기체 상태로 존재하는 대신 액체 상태로 존재했을 것이다. 그 결과 우리가 전혀 알지 못하는 새로운 액체를 만들어 냈을 것이다.”
– 앙투앙 라부아지에Antoine-Laurent de Lavoisier, 1743-1794
생명의 기원, 물
주변을 둘러보라, 무엇이 보이는가? 육상 동물인 우리 주변에는 흙, 돌, 나무부터 콘크리트, 유리, 알루미늄, 구리, 스테인리스 스틸, 플라스틱, 고무 등 스스로 형체를 유지하고 있는 수많은 고체가 눈에 띈다. 그 외에 또 뭐가 있을까? 우리 주변을 가득 채운 공기는 무색무취의 기체이고 가장 흔한 액체는 물론 물, 즉 H2O이다. 독자들의 책상에 있을 법한 커피, 차, 우유, 주스, 탄산 음료 등은 적어도 85% 이상의 물에 다른 성분이 조금 섞여 있는 액체일 뿐이다. 꿀 또는 설탕 시럽이 거의 예외적으로 물보다 다른 물질(설탕)이 더 많이 포함된 액체라고 할 수 있다. 대부분의 수용성 물질도 물에 섞이지 않은 상태에선 액체 상태로 존재하지 않는다. 예를 들면 각설탕은 물에 잘 녹지만 자체적으로는 고체 상태로 존재한다. 일상 생활에서 ‘액체’와 ‘물’은 거의 동치에 가깝다.
인간 몸의 70%가 물인 만큼 단일 물질로서 인간(뿐만 아니라 모든 생명체)에게 가장 중요한 것 역시 물이다. 물은 생명을 이루는 핵심 물질이고 지구상에 생명체가 존재할 수 있었던 이유 또한 물이 존재하기 때문이다. 생명체의 중요한 특성 중 하나는 형체와 기능이 변화할 수 있다는 것이고, 그러려면 반드시 액체가 필요하다. 고체와 구별되는 액체의 큰 특징은 스스로 형체를 유지할 수 없다는 점이다. 생명체의 몸이 로봇과 달리 다양한 모양으로 부드럽게 변형이 가능한 것은 몸체가 액체, 즉 물 기반이기 때문이다.
물이 생명체에게 있어서 중요한 또 다른 특성은, 물 분자가 갖고 있는 ‘극성’이다. 두 개의 수소 원자가 한 개의 산소 원자와 결합해서 물 분자를 만들 때, 두 수소 원자는 한쪽으로 쏠리면서 비대칭적인 구조를 이룬다. 그 결과 물 분자의 전하 분포 역시 산소 원자 주변은 음극, 두 수소 원자 주변은 양극을 띄는데, 이런 식으로 한 분자 속에서 전하 분포가 비대칭성을 띄는 현상을 극성이라 한다.
이런 극성 덕분에 물 분자는 다른 물 분자들을 포함해서 극성을 띄는 다양한 분자들과 강하게 상호작용을 한다. 그 결과 물에는 많은 물질이 녹기 때문에 물을 흔히 범용 용매universal solvent라고도 한다. 생명체는 범용 용매의 특성을 적극적으로 활용하여 생존에 필요한 다양한 기능을 수행하는 물질을 생명체 곳곳으로 수송한다. 화성에 물의 흔적이 있느냐 없느냐가 뉴스 거리가 되는 이유 역시 물의 존재 여부가 외행성에서 생명체의 존재를 확인하기 위한 첫걸음이기 때문이다.
우리 주변에 물을 제외한 다른 액체는 뭐가 있을까? 실험 과학자가 직업이 아닌 이상, 인간이 살면서 마주할 수 있는 액체는 기름, 알콜, 산으로 분류되는 물질 중에서도 극히 일부에 불과하다. 설령 술을 무척 좋아하는 애주가라 하더라도 순수한 알콜 섭취량은 하루에 머그잔 한 잔을 넘지 못한다. 반면 인간이 다양한 경로로 섭취하는 물의 양은 하루 평균 3L 정도나 된다. 물은 인간에게 너무나도 중요한 물질인 나머지, 지루할 정도로 흔한 물질이다. 화학의 아버지로서 다양한 물질을 다루어 봤던 라부아지에 입장에서 액체의 세상은 얼마나 단조로왔을까. 왜 ‘새로운 액체’를 만들어 내고 싶었을지 상상이 간다.
가열과 냉각
지구 표면의 70%가 바닷물로 덮여 있다고 하지만 바다 깊숙이 들어가 보면 밑에는 결국 딱딱한 지각이 자리 잡고 있다. 지각 깊숙한 곳에 있는 지구 부피의 15% 정도를 차지하는 핵은 대부분 철이 녹은 액체 상태로 존재한다. 지구의 핵과 지각 사이에는 지구 부피의 84%를 차지하는 맨틀이 있는데, 지금의 맨틀은 실리콘 기반의 돌덩이에 가깝지만 고생대까지만 해도 액체 상태로 존재했다. 지구의 나이를 45억 년이라고 보면 90% 이상의 시간 동안 지구는 얇은 껍질 속에 아주 뜨거운 액체가 담겨 있는, 계란과 같은 상태였다.
오늘날의 지구는 45억 년 전 철과 규소가 녹아서 뒤섞인 커다란 액체 방울이 표면부터 서서히 식어가면서 딱딱한 껍질을 만들어 낸 결과물이다. 우리 인간이 아직 존재하지 않았던 초기 지구에는 지금 우리가 볼 수 없는, 물이 아닌 액체가 지천에 널려 있었으리라. 비록 우리가 일상적으로 접하진 못하지만 그렇다고 뜨거운 액체가 꼭 우리에게 낯설지는 않다. 영화 <터미네이터 2>의 마지막 장면이 설득력을 얻는 것도 결국은 섭씨 천 도가 넘는 용광로 속에서 붉게 빛나는 금속 액체에 대한 친숙함 덕분이다.
글의 서두에서 인용한 라부아지에의 말에는 그 자신도 깨닫지 못한 상당한 통찰이 담겨 있었다. 고체를 뜨겁게 달궈 액체를 만드는 게 가능하다면, 반대로 (라부아지에의 상상처럼) 우리에게 친숙한 기체를 차갑게 냉각해 액체로 바꾸는 것 역시 가능할 텐데, 막상 기체를 액체로 만드는 장면은 터미네이터의 용광로처럼 익숙한 이미지로 남아 있지 않다. 왜 그럴까? 다양한 이유를 찾을 수 있겠지만, 필자의 생각에 궁극적인 차이는 가열과 냉각 기술 사이의 비대칭성에 있다. 주머니에 넣을 수 있는 라이터 하나만 켜도 몇백 도의 온도에 도달할 수 있고, 이를 잘 활용하면 물도 끓일 수 있지만, 그 반대로 물을 얼릴 수 있는 휴대용 도구는 존재하지 않는다.
실제로 고대 인류가 불을 사용한 흔적은 1-2백만 년 전으로 거슬러 올라간다. 불로 섭씨 수백도 정도까지는 일상적으로 도달할 수 있었을 테고, 불을 이용하여 섭씨 1000도와 1500도에 도달할 수 있게 됐을 때 각각 청동기와 철기 시대가 열렸음을 떠올려 보면, 인류 문명 발달에 있어서 금속을 녹일 수 있는 기술의 중요성은 아무리 강조해도 지나치지 않다. 인류 역사상 가장 짧은 기간 안에 가장 놀라운 기술적 발전을 이뤄낸 산업 혁명의 핵심이 증기기관, 즉 엔진의 발명이라고 한다면, 발명의 밑바탕에는 금속 제련 기술과 이를 가능하게 해준 불을 사용한 가열 기술이 자리 잡고 있었다. 게다가 증기기관을 운용하기 위해 증기를 생산하려면 물을 가열하여 끓일 수 있어야 했으니, 여러모로 가열 기술은 쓸모가 많았고, 상당히 발달해 있었다.
반면 냉각 기술은 어떨까? 냉장고와 에어컨이 없는 세상을 경험해보지 못한 독자가 대다수일 것이다. 하지만 능동적 냉각 기술은 불과(?) 백여 년 전 산업혁명이 일어난 뒤에나 가능해진, 인류 역사를 놓고 보면 상당히 최근에 얻어진 첨단 기술이다. 대학교에서 가르치는 일반 물리학에는 열역학이란 단원이 있는데, 여기서 학생들은 “엔진을 거꾸로 돌리면 냉장고가 된다”고 배운다. 즉, 산업혁명의 모태가 된 엔진의 개발이 있었기에 그 역과정이라 할 수 있는 냉장고의 개발도 가능했다는 뜻이다.
인류 최초의 냉장고는 1834년 제이콥 퍼킨스Jacob Perkins, 1766-1849가 만들었으며 ‘아이스 머신’이라고 불렀다. 당시의 냉장고는 에테르를 냉매로 사용하는 증기 압축 냉동기로서, 이름이 암시하듯 간신히 얼음이나 얼릴 정도의 냉동기였다. 당시 이미 금속 제련을 위해 수천도의 온도에 손쉽게 도달할 수 있었음을 감안하면 겨우 30도 정도 냉각하는 기술의 비루함은 명확해진다. 그런 이유로 18세기에 이미 라부아지에가 기체를 액화시키는 상상을 했음에도 불구하고 막상 공기를 액체로 만드는 데에는 그로부터 100년 이상의 시간이 걸렸다.
액체란 무엇인가?
기체를 액체로 만들고 싶으면 일단 두 물질 사이의 차이점이 뭔지 알아야 한다. 우리에게 익숙한 물질의 세 가지 상태 사이에는 확연히 구분되는 특성이 있다. 우선 고체는 형체가 정해져 있다는 점에서 액체나 기체와 구분된다. 액체와 기체는 이들을 담고 있는 (고체) 용기에 의해서 형상이 결정된다. 이런 점에서 액체와 기체는 매우 유사하여, 이를 묶어서 흐르는 물체라는 의미로 유체流體라고 부르기도 한다. 이런 유사성에도 불구하고 우리는 액체와 기체를 손쉽게 구분할 수 있다.
왜 그럴까? 일단 액체는 무겁다. 두 물질의 밀도 차이 때문이다. 바꿔 말하면 기체는 입자(원자나 분자)의 크기에 비해 입자간 거리가 굉장히 먼 반면 액체는 입자의 크기와 입자간 거리가 비슷하다. 멀리 떨어져 있는 두 개의 당구공 사이의 거리는 얼마든지 더 줄일 수 있지만, 서로 맞닿아 있는 당구공 사이의 거리를 더 줄이기란 쉽지 않다. 원자나 분자가 이렇게 유한한 크기를 갖는 단단한 입자라고 생각한다면, 두 물질 상태의 압축률(힘을 가해서 얼마나 압축이 잘 되는지 여부)에 따라 기체와 액체를 구분할 수도 있다. 이런 사실에 착안하여 기체를 계속 압축하다 보면 더 이상 압축이 되지 않는 액체로 만들 수 있을 것만 같은 기분이 든다.
실제로 이런 원리를 이용하여 1823년 험프리 데이비Humphrey Davy, 1778-1829와 마이클 패러데이Michael Faraday, 1791-1867는 염화수소물chlorine hydrate, Cl2・10H2O에 포함된 염소Cl를 액화하는 데 성공했다. 이를 위해 고체 상태인 염화수소물을 [그림1과] 같이 ㄱ자 모양의 밀봉된 유리튜브에 넣고 이를 가열한다. 그러면 이 고체가 승화되면서 기체로 변하는데, 그렇게 상승한 압력으로 인해 ㄱ자 튜브의 반대쪽에 염소 액체가 모이는 것을 확인한 것이다. 이게 상온, 상압에서 액체로 존재하지 않는 물질을 액화시킨 최초의 기록 중 하나이다. 데이비와 패러데이의 성공 이후 패러데이 스스로 암모니아를 비롯한 6종류의 기체를 액화시킨 것을 포함하여, 많은 이들이 다양한 기체를 액체로 만드는 데 성공하였다.
비록 데이비와 페러데이가 기체를 액화하는 방법을 발견하긴 했지만, 이는 본래 라부아지에가 생각했던 방식과는 조금 다른 방법을 통한 성공이었다. 우리는 경험을 통해 물 분자의 온도를 높여주면 얼음-물-수증기 순서로 상태가 변한다는 사실을 알고 있다. 아주 낮은 온도에서 입자의 운동이 거의 없을 때는 입자들의 상대적 위치가 고정된 고체 상태로 존재하다가 열에너지를 넣어주면 차츰 입자들의 운동이 커지면서 입자들이 자유롭게 움직이는 액체로 바뀐다. 그러다가 더 많은 에너지를 넣어주면 더욱 운동의 폭이 커지면서 서로 더 멀리 떨어질 거라고 상상할 수 있다. 이게 바로 라부아지에의 상상이었다.
반면 1800년대 중반까지 기체를 액화하는 데 사용한 과정은 데이비-페러데이처럼 기체에 압력을 가하여 부피를 줄이다 보니 기체가 액체로 바뀐 것이었다. 기체 상태에 많은 압력을 가하다 보니 입자들의 운동이 억제되어 액체로 바뀌었다고 보면 된다. 현실 세계에서 고체-액체-기체 상태를 바꾸는 데 효율적인 손잡이knob가 온도와 압력이다.1
영구 기체와 판 데르 발스
당대의 과학자들을 당황하게 만든 것은 1800년대 중반까지 약 20년간의 노력에도 불구하고 지구상에서 가장 흔한 기체인 공기를 액화할 수 없었다는 점이다. 공기를 이루는 가장 흔한 기체 세 가지, 질소와 산소, 아르곤, 그 외에도 수소, 일산화탄소 등의 기체는 좀처럼 액화가 되지 않았다. 그래서 포기가 빠른 일부 과학자들은 이들 몇몇 기체를 영구 기체permanent gas라고 여기기도 하였다. 그렇지만 이는 순전히 고체-액체-기체 상전이 그림([그림2])에 대한 이해가 부족한 까닭이었다.
영구 기체에 대한 오해를 1860년대에 실험적으로 바로 잡은 이가 토마스 앤드류즈Thomas Andrews, 1813-1885이고, 요한네스 판 데르 발스Johannes van der Waals, 1837-1923가 오래지 않아 이에 대한 깔끔한 해석을 내놓았다. 판 데르 발스는 그 공로로 1910년에 노벨 물리학상을 수상하였다.
이들의 업적에 대해 이야기하기 전에 다음과 같은 사고 실험을 해보자. (물론 시간과 돈이 있다면 실제 실험을 해봐도 좋다.) 카메라가 설치되어 있는 방 안에 진공을 잡고, 투명한 기체나 액체 중 딱 한 가지를 골라서 방을 가득 채우고 밀폐한다. 그리고 카메라로 방 내부를 촬영을 한 영상만을 통해서 방 안에 액체가 들어 있는지 기체가 들어있는지 구분할 수 있을까? 꼭 할 수 있을 것만 같다. 고프로를 이용하여 스키를 타며 찍은 영상과 스쿠버 다이빙하며 찍은 영상은 주변이 한 가지 매질(공기와 물)로 가득 차 있음에도 확연히 구분 가능하지 않은가?
여기서 두 영상을 구분 가능하게 해주는 요소가 무엇인지를 생각해 볼 필요가 있다. 우선 주변 동식물의 움직임, 빛의 양과 일렁임 등을 통해 이를 구분할 수 있다. 우리가 주변 요소들의 변화에 의존하지 않고 기체와 액체 상태를 정확히 구분해내기란 대단히 어렵다. 그럼에도 불구하고 우리가 일상에서 이를 구분하는 데에 있어서 어려움을 겪지 않는다. 텅 빈 유리잔과 물이 찬 유리잔을 헷갈리는 사람은 없다. 이를 구분할 수 있는 결정적인 단서는“경계면”의 존재 유무이다. 앞서 언급한 바와 같이 기체와 액체 사이에는 상당히 큰 밀도 차이가 있다. 이렇게 밀도 차이가 심하게 나는 액체와 기체가 공존하는 경우에 밀도가 높은 액체가 아래에 가라앉고, 기체가 위에 뜨면서 명확한 경계면이 생긴다. 이 경계면을 확인할 수 있을 때 같은 물질이라도 두 개의 서로 다른 상태에 존재한다는 것을 알 수 있다. 기체를 압축하여 액체를 만드는 상황에서도 ‘아, 이제 기체가 액화되었구나’하고 알 수 있는 것은 경계면을 확인할 수 있을 때이다.
이런 경계면이 생기는 이유가 뭘까? 기체를 압축해 밀도를 높이다 보면, 액체의 밀도와 같아질 때까지 기체 밀도가 연속적으로 높아지는 게 아니다. 그 대신 어떤 특정 압력에서 밀도가 불연속적으로 급격히 높아지면서 기체가 액체로 바뀌는 일이 벌어진다. [그림2]의 파란선을 따라 1→3 방향으로 압력을 서서히 높여주는 상황을 상상해 보자. 이는 투명한 유리병에 기체를 가득 채운 뒤 피스톤으로 눌러주는 상황과 같다. 처음 한동안은 육안으로 구분되는 변화가 없다가, 압력이 일정한 값에 도달하면 갑자기 유리병에 액체가 고이기 시작하는데, 이게 파란선의 2번 점에 도달했을 때이다. 여기서 압력을 더 올려주면 물질은 완전히 액체로 바뀌게 된다.
온도-압력 상전이 그림에서 두 가지 상태, 예를 들어 액체와 기체 상태를 구분 짓는 경계선이 있는데, 이를 액체-기체 공존선이라고 부른다. 액체-기체 공존선의 정확한 모양은 물질에 따라 다르지만, 모든 물질에서 예외 없이 온도-압력 상전이 그림에서 우상향의 모양을 띈다. 공존 곡선의 하단이나 우측에 있을 때 물질은 완전히 기체 상태로만 존재하고, 그보다 좌측이나 상단에 있을 때는 완전히 액체 상태로만 존재하지만 공존 선상을 따라서는 액체와 기체가 공간적으로 명확한 경계면을 이루면서 공존하는 양상을 보인다.
온도가 낮아지다 보면 물질은 거의 예외 없이 고체로 바뀌기 때문에 고체 상태가 액체-기체 공존선을 가로막는 경우가 있다. 이럴 때면 물질이 액체-기체 상태로만 공존하는 것이 아니라, 고체-액체-기체 세 가지 상태로 모두 공존할 수 있기에, 이를 물질의 삼중점이라고 한다. 액체-기체 공존선을 따라 온도와 압력을 계속 올리다 보면 제4의 물질이 등장하지 않음에도 액체-기체 공존선이 끝나는 점이 있고, 이 점을 임계점이라고 한다. 이 임계점에서는 무슨 일이 일어날까?
액체-기체 공존선의 의미를 잘 생각해 보면, 공존선을 경계로 밀도 차이가 명확하게 나는 두 가지 물질상태, 액체와 기체가 존재한다. 같은 액체 상태라고 하더라도 압력을 일정하게 유지하면서 온도를 높이면 입자의 운동이 많아지고 그 결과 액체의 밀도가 점점 낮아질 거라고 짐작할 수 있다. 즉, 온도가 높은 액체는 온도가 낮은 액체에 비해 밀도가 낮다.
또한 같은 기체 상태에서도 온도를 일정하게 유지하면서 압력을 높이면 기체의 밀도는 낮아진다. 따라서 높은 온도의 액체는 밀도가 낮아지고, 높은 압력의 기체는 밀도가 높아지는 특성 때문에 온도와 압력이 모두 충분히 높은 특정 지점에서는 액체와 기체를 구분시켜주는 밀도 차이가 사라지는 점이 생길 거라 상상할 수 있다. 이렇게 액체와 기체의 구분이 사라지는 점이 바로 상전이 그림 상의 임계점이다. 이 임계점의 존재를 실험적으로 밝혀낸 이가 앤드류즈이고, 우리가 중학교 때 배우는 이상 기체 상태 방정식을 아주 살짝 수정한, 간단하다면 간단한 이론으로 임계점의 존재와 액체-기체 상전이를 설명해 낸 이가 판 데르 발스였다.
임계점의 발견을 통해 얻은 교훈은 기체가 액화되는 과정을 관측하려면 반드시 임계온도보다 낮은 온도에서 기체를 압축해야 한다는 점이었고, 소위 영구 기체의 비밀(?)도 알고 보니 바로 임계온도에 숨어 있었다. 임계온도는 물질마다 다른데 질소, 산소, 아르곤, 수소의 임계온도는 각각 섭씨 −147도, −119도, −122도, −240도이다. 그러다 보니 상온에서 압축을 통해 기체가 액체로 바뀌는 현상을 관측할 수 있을 리 만무했다. 비슷한 시기에 개발된 제이콥 퍼킨스의 아이스머신 따위(?)로는 엄두도 낼 수 없는 온도였으니, 한동안 공기는 액체로 변하지 않는 “이상 기체”로 이뤄졌다고 상상했을 법도 하다. 뒤집어 말하면 임계점의 존재와 그 의미를 깨닫고 나니, 기체를 우선 충분히 냉각할 수 있다면 공기의 액화도 가능하리라 짐작할 수 있다. 그리고 액화를 위한 경쟁은 급속한 냉각 기술의 발전을 이끈다.
공기 액화의 길
열역학은 참으로 기묘한 방법으로 인간에게 성공의 길을 열어 주었으니, 압축을 통해 새로운 액체를 일단 한 번 만들면 그 액체를 이용해 이전에는 도달할 수 없었던 온도까지 냉각할 방법이 생겨난다는 점이다. 목욕을 하고 난 뒤 몸이 젖은 상태에서 바람이 불면 몸이 시원해지는 경험은 누구나 있을 것이다. 이것은 물이 기화될 때 주변으로부터 기화열을 흡수하여 온도가 낮아지는 현상으로, 정온동물이 더울 때 땀을 흘려 체온을 유지하는 원리이기도 하다. 이와 같이 액체가 기체로 바뀔 때 주변으로부터 에너지를 흡수하는 현상은 모든 물질에서 공통적으로 나타나는데, 이를 이용한 냉각 기술을 기화 냉각evaporative cooling이라고 한다.
기화 냉각을 적극적으로 활용하는 방법으로, 액체를 담아 둔 용기에 펌프로 진공을 만들어주는 길이 있다. 액체가 담겨 있는 용기에 진공 펌프를 연결하면 용기 내부의 압력이 낮아지면서 액체의 일부가 순간적으로 기화되고 기화열로 인해 액체의 온도가 낮아진다. 이런 기화 냉각법은 앞서 설명한 상전이 그림의 액체-기체 공존선을 이용하면 쉽게 이해할 수 있다. 액체가 담긴 용기의 압력을 낮추더라도 액체 전체가 기체로 바뀌기 전까지는 액체와 기체가 공존하는 상태이다. 따라서 물질은 액체-기체 공존선을 벗어날 수 없다. 액체-기체 공존선은 좌하향-우상향의 곡선이므로 액체-기체 공존선을 따라서 액체의 압력을 낮추면 액체의 온도도 함께 낮아진다. 이런 기화 냉각법은 용기 내부의 액체가 모두 기화되거나, 상전이 그림의 삼중점을 만나 액체가 고체로 바뀔 때까지 물질에 적용할 수 있다.
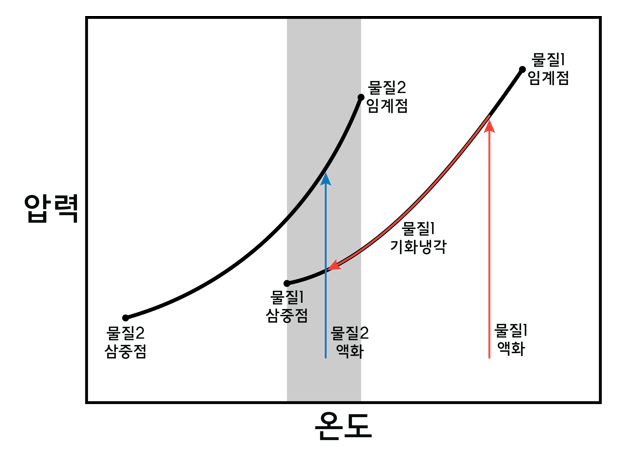
이 원리를 응용하면, 어떤 물질의 임계온도가 비록 상온보다 아주 낮더라도 다른 물질의 삼중온도보다 높기만 하다면 액화할 방법이 생긴다. [그림3]의 회색 영역과 같이 두 물질의 액체-기체 공존선 중 서로 겹치는 온도구간이 존재할 경우를 생각해 보자. 일단 첫 번째 물질을 액체로 만들고 기화 냉각을 통해 회색 영역까지 온도를 낮춘다. 그리고 기체 상태의 두 번째 물질을 낮아진 온도에서 압축하면 액화시킬 수 있다. 적당한 물질을 찾아서 이런 과정을 반복적으로 수행하면 임계온도가 매우 낮은 물질도 액화시키는 것이 가능하고, 이런 냉각 기법을 단계 냉각법cascade cooling이라 한다.
이런 단계 냉각법을 적절히 활용한 덕분에 1877년 스위스의 라울 픽테Raoul Pictet,1846-1929와 프랑스의 루이 까이예테Louis Cailletet, 1832-1913는 처음으로 산소를 섭씨 영하 183도에서 액화하는 데 성공한다. 공기의 20% 정도를 액화하는 데 성공한 셈이다. 1883년, 폴란드의 지그문트 브루블레브스키Zygmunt Wróblewski, 1845-1888와 카롤 올스제브스키Karol Olszewski, 1846-1915가 질소 액화(액화점 −196도)에 성공함으로써 인류는 공기의 99% 이상을 액체로 만들 수 있게 되었다. 산소를 액화하기까지 라부아지에 사후 거의 100년, 데이비와 패러데이가 염소를 액화한 지 50년 이상이 걸렸지만, 이후 질소를 액화하는 데에는 불과 6년도 채 걸리지 않은 것을 보면, 산소 액화가 “영구 기체”들을 액화하는 방법을 개발하는 데에 있어서 얼마나 결정적인 역할을 했는지 알 수 있다.
그런 의미에서 산소를 액화한 것이 완전히 새로운 종류의 액체를 만들 수 있을 거라는 라부아지에의 비전이 실현되는 순간이었다고도 할 수 있는데, 실제로 액체 산소는 라부아지에의 비전에 어울리는 신기한 액체이기도 하다. 액체 산소는 [그림4-1]에서 볼 수 있는 것과 같이 오묘한 푸른 빛을 띈다. 또한 산소는 액체 상태에서 상자성 물질로 [그림4-2]처럼 자석에 붙기도 한다. 마지막으로 산소는 매우 반응성이 높은 물질로 연소의 3요소로 꼽히는 물질인 만큼 밀도를 매우 높인 액체 상태에서 엄청난 반응성을 보인다. 공기 중에서는 어지간해서 철수세미에 불을 붙일 수 없지만 철수세미에 액체 산소를 부어서 불을 붙이면 활활 탄다. 필자도 대학원 시절에 친구들과 직접 시도해본 적이 있는데, 필자의 대학원 지도 교수님이 수업 시간에 이를 시연하다가 강의실 강의대에 구멍을 뚫었다는 이야기는 도시 괴담처럼 전해져 내려오고 있다.
그에 비하면 액체 질소는 굉장히 차갑다는 것 외에 별다른 눈에 띄는 특징이 없다. 그렇지만 질소가 공기의 80%를 차지하는 대단히 안정적인 물질이고, 공기는 우리 주변에 어디나 있다는 점 자체가 장점이기도 하다. 액체 질소 1리터는 몇백 원 수준으로 생수보다도 싸게 살 수 있고, 대단히 안정적인 물질이다 보니 오늘날에는 다른 물질을 섭씨 영하 200도 가까이 냉각시키기 위한 저온 냉매로 널리 사용되고 있다.
세상에서 가장 차가운 액체
19세기 말, 과학계에서 가장 중요한 과제 중 하나는 질소와 산소뿐만 아니라 생각할 수 있는 모든 기체를 액화하는 것이었는데, 일단 원리를 깨닫고 나자 나머지 기체를 액체로 만드는 일은 시간 문제처럼 보였다. 당시에도 잘 알려진 사실 중 하나는 일반적으로 원자량이나 분자량이 작을수록 액체의 끓는점이 낮다는 점이었다. 게다가 끓는점이 유난히 낮은 불활성 기체의 존재에 대해서는 1890년대 중후반까지도 아무도 몰랐기 때문에, 많은 이들이 생각한 ‘영구기체’ 액화의 종착역은 수소를 액화하는 것이었다.
그렇지만 막상 수소를 액화하는 과정에서 큰 장애물에 부딪쳤다. 당시에 단계 냉각으로 도달할 수 있는 가장 낮은 온도는 대략 −220도 정도였는데 수소의 임계온도는 −240도로 이보다 20도가량 낮았다. 따라서 단계 냉각 후 압축만을 통해 수소를 액화할 수는 없었다. −220도에서 −240도까지 기체 상태의 수소를 냉각할 새로운 방법이 필요했다.
당시에 줄-톰슨Joule-Thomson 효과를 이용하여 기체의 온도가 낮아진다는 것이 알려져 있었기 때문에 −220도에서 출발하여 줄-톰슨 효과를 통해 수소를 액화하려는 시도도 있었다. 줄-톰슨 효과란 기체가 좁은 노즐이나 작은 구멍을 통과할 때 온도가 낮아지는 현상이다. 자전거 바퀴에서 바람을 빼거나, 컴퓨터/전자제품 청소용 깡통을 사용해 본 사람이라면 바람이 빠지는 과정에서 자전거 바퀴나 깡통이 차가워지는 걸 경험해 본 적이 있을 텐데, 이게 바로 줄-톰슨 효과이다.
문제는 또 있었다. 차갑디차가운 수소 액체를 모아 둘 용기를 충분히 낮은 온도로 냉각시키는 것이 어려웠다. 이 문제를 해결한 이는 스코틀랜드 화학자 제임스 듀어James Dewar, 1842-1923였다. 픽테와 까이예테가 산소 액화에 성공한 같은 해에 듀어는 영국 왕립 연구소Royal Institute의 Fullerian Professor로 임명되어 패러데이의 성공적인 업적을 이어갔다. 듀어는 1892년 유리로 된 최초의 진공 보온병을 개발하여 외부에서 용기로 들어오는 열을 차단하였고, 수소 자체의 줄-톰슨 효과로 보온병 내부의 온도를 충분히 낮추는 데에 성공하였다. 그 결과 1898년 수소를 액화(액화점 −253도)하는 데 성공한다.
여담이지만 듀어의 이름을 따서 실험실에서 사용하는 대형 저온 액체 보관 용기를 아직도 ‘듀어’라고 하지만, 일반인들에게는 진공 보온병은 듀어보다는 써모스라는 이름으로 훨씬 익숙할 것이다. 듀어는 자신이 개발한 진공 보온병에 대해 과학적 실험 도구 이상으로서의 중요성을 알아채지 못하여 이에 대한 특허 등록을 하지 않았고, 독일인 유리 세공인glass blower 두 명이 이 기술을 이용하여 회사를 차렸는데, 그 회사가 바로 써모스Thermos이다. 듀어는 뒤늦게 써모스를 상대로 소송을 했지만 등록해놓은 특허가 없었기에 패소하였고, 결국 자신의 발명품으로 돈을 한 푼도 못 벌었다.
이제 인류가 액체와 고체로 만들지 못한 마지막 기체는 1895년 이후에 발견된 헬륨, 네온, 아르곤 등의 불활성 기체들 몇 개만이 남았다. 아르곤과 네온의 액화점은 수소보다 높기 때문에 크게 어려움이 없었지만 헬륨은 (원자량이 수소의 분자량보다 큼에도 불구하고) 쉽게 액화되지 않았다. 수소 액화를 선점한 듀어는 헬륨 액화도 본인이 해낼 수 있을 것이란 자신감이 있었다. 그렇지만 정작 헬륨 액화를 처음으로 성공한 것은 네덜란드의 카멜링 온네스Kamerling Onnes,1853-1926로 1908년에 액체 수소보다도 15도 이상 낮은 영하 269도에서 헬륨을 액화하는 데 성공하였다.
더욱 놀라운 것은 그 이후로도 무려 15년간 아무도 헬륨을 액화하는 데 성공하지 못하면서, 헬륨 액화 기술을 온네스가 독점했는 점이다. 심지어 1923년에 두 번째로 헬륨 액화에 성공한 토론토 대학의 존 맥레넌John McLenan, 1867-1935도 온네스에게 대량의 기체 헬륨을 넘겨주고 그 대가로 온네스의 액화기 설계도를 넘겨 받아 액화기를 제작하는 데 성공했다고 한다. 오늘날 어떤 연구실에서 개발한 기술을 15년 동안 독점한다는 건 도저히 상상이 가지 않는다. 어째서 이런 일이 가능했을까?
이에 대해서는 대개 두 가지 이유를 중요하게 꼽는다. 첫 번째는 당시 온네스를 돕던 숙련된 기술자 무리를 꼽아야 할 것이다. 단계 냉각과 줄-톰슨 효과를 이용하여 기체를 액화하기 위해서는 기체에 높은 압력을 가할 수 있는 가압 기술, 압축을 통해 생성된 액체의 압력을 낮춰 기화 냉각을 유도하기 위한 진공 기술, 영하 200도 이하의 온도를 유지할 수 있는 단열 기술 등이 복합적으로 요구된다.
게다가 당시에 단계 냉각을 위해 사용된 아세틸렌 등은 가연성 물질로 기체 상태에서도 충분히 위험한데, 이를 고밀도의 액체 상태로 포집하고 이를 이용해서 연소를 일으키는 산소마저 고밀도 액체로 만드는 등, 온갖 위험이 도사리는 실험이었다. 실제로 듀어의 실험실에서 발생한 폭발 사고로 그의 오른팔이었던 로버트 레녹스Robert Lennox는 한쪽 눈이 실명되기도 하였다. 이처럼 저온 기체 액화 실험을 제대로 수행하기 위해서는 당시 기술 수준에서는 거의 공장 규모의 인력과 설비가 필요했는데, 아무리 뛰어난 실험가라고 하더라도 이런 기술과 장비들을 한 사람이 모두 숙련되게 익혀서 운용하기는 불가능하였다.
게다가 대부분의 ‘대학’들은 이런 대규모 실험 설비와 인력의 중요성을 이해하지 못했다. 수소 액화에 최초로 성공하면서 유리한 고지를 선점한 것은 듀어였지만, 약간의 수소를 액화하는 데 성공하는 것과 헬륨 액화를 위한 예비 냉매pre-cooling agent로 사용할 수 있을 정도로 대량의 수소를 액화하는 것은 전혀 다른 문제다. 듀어에게는 자신의 성공을 대규모로 확장할 여력과 환경이 주어지지 않았다. 듀어의 조수인 레녹스는 매우 훌륭한 기술자였지만, 그 외에는 도와줄 수 있는 사람이 많지 않았다. 게다가 듀어는 그런 레녹스와의 관계마저도 잘 유지하지 못하였다. 급기야 온네스가 헬륨 액화에 성공한 이후로 두 사람의 관계는 급속도로 악화되었고, 레녹스는 듀어가 영국 왕립 연구소Royal Institution에 있는 한 자신은 그곳에서 어떤 일도 하지 않겠다며 떠났다고 한다. 듀어는 실험을 제대로 하기 위해서는 거의 모든 것을 직접 관장해야만 했던 고충에 대해 토로하기도 하였다.
그에 반해 온네스는 게릿 플림Gerrit Flim이 이끄는 (당시 그들이 입고 있던 푸른 복장 때문에) ‘푸른 소년들blauwe jongen’이라는 별명을 가진 숙련된 기술자들을 한 부대 데리고 있었다. 이들은 기체 액화 기술의 난이도에 대해 충분히 인지한 온네스가 1880년대부터 공들여 양성한 젊고 잘 훈련된 기술자들이었는데, 1898년에는 16명이었던 푸른 소년들은 1904년에는 32명으로 늘어났다. 이들은 고압·진공 장비 및 부품의 관리 및 개조를 맡았고, 그 외에 오스카 케셀링Oskar Kesselring처럼 유리를 불어서 원하는 형태의 용기를 만드는 유리직공들의 역할도 필수적이었다. 본인이 마주한 과업의 규모와 범위를 파악하고 이에 따라 인력을 키워낼 수 있었던 온네스의 선견지명도 놀랍지만, 이런 그의 노력을 묵묵히 지원해준 라이덴 대학의 풍토 역시 상당히 놀랍다. 기체 액화 이론의 선구자였던 판 데르 발스가 당시에 라이덴 대학에 함께 있었다는 점 역시 이를 가능케 해준 요인이 아니었을까 싶다.
온네스의 독점적인 성공의 두 번째 이유는 액화할 양질의 헬륨을 확보할 수 있었다는 점이다. 이 부분에서는 듀어가 훨씬 유리한 위치를 차지할 수도 있었지만 그러지 못했다. 1895년 헬륨을 발견한 화학자는 스코틀랜드 출신의 윌리엄 램지Sir William Ramsay, 1853-1916였는데, 이를 효과적으로 정제하기 위해 저온 액화기를 필요로 했다. 램지가 제임스 듀어에게 도움을 청했더라면 듀어가 헬륨을 액화하는 데 있어 엄청난 우군이 될 수 있었지만, 불행히도 듀어와 램지는 사이가 매우 나빴고, 램지는 윌리엄 햄슨William Hampson, 1854-1926과의 협력을 선택했다.
햄슨은 대량으로 기체를 액화할 수 있는, 오늘날 린데-햄슨 순환 방식으로 알려진 방법을 개발한 냉각 액화 기술의 전문가였지만, 그의 관심사는 더 낮은 온도에 도달하는 것보다는 더 효율적인 액화 기술 개발이었던 것 같고, 그가 헬륨 액화에 관심을 가졌던 것 같지는 않다. 그러는 사이에 카멀링 온네스는 그의 동생 온노 온네스Onno Onnes, 1861-1935의 협조로 다량의 헬륨을 확보하는 데 성공하였다. 당시 암스테르담의 Office of Commercial Intelligence의 중역이었던 온노 온네스는 형에게 미국 노스 캘로라이나에서 생산된 다량의 모나자이트를 구해주었고, 카멜링 온네스는 모나자이트로부터 약 300리터의 기체 헬륨을 추출하는 데 성공하였다.
그 결과 헬륨 액화 경쟁은 온네스의 압도적인 승리로 끝이 난다. 또 한 가지 아이러니는 램지가 헬륨을 발견한 시점이 영구 기체를 액화하기 위한 경주가 끝을 향해 가던 1895년이었다는 점이다. 이 시기에 그가 헬륨을 발견하지 못했더라면, 즉 헬륨이 존재하지 않았더라면 마지막 남은 영구 기체인 수소를 액화한 영광은 듀어에게 돌아갔을 것이다. 램지와 듀어의 악연은 여러모로 얄궂다. 하지만 역사에 만약은 없는 법이고, 온네스마저도 듀어의 진공 용기 개발이 저온 액화 기술의 핵심이었다고 인정했음에도, 저온 물리학의 역사는 듀어가 아니라 온네스와 함께 시작되었다고 받아들여지고 있다.
그 이유는 온네스의 업적이 단순히 액화할 수 있는 가장 낮은 온도의 물질을 액체로 만드는 데 성공한 것에 그치지 않았기 때문이다. 온네스의 업적이 그 정도의 중요성뿐이었다면, 그가 헬륨 액화 기술을 15년 동안이나 독점했다는 사실도 그다지 놀라울 게 없었을 것이다. 헬륨 액화는 그저 호기심 많은 과학자 무리 사이에서 벌어진 ‘쓸데없는’ 일이었고, 누군가 고지를 점령한 순간 더 이상 그 길을 따라가야 할 이유가 없는 일이었을 테니까.
하지만 온네스의 헬륨 액화와 함께 마무리가 됐어야 할 라부아지에의 꿈은 그와 동시에 역사적 전환점을 맞이한다. 온네스는 액체 헬륨을 바탕으로 두 가지 중요한 발견을 하게 된다. 그중 하나는 초전도체의 발견이고, 다른 하나는 액체 헬륨은 절대 영도에서도 얼지 않는 ‘영구 액체’라는 사실이었다. 두 발견이 가져다준 어마어마한 양자역학적 통찰과 그 이후 물리학의 발전에 대해서는 다음 이야기에서 다루기로 한다.