들어가며
유리를 연구하는 국내 한 대학의 교수에게 들었던 일화다. 본인이 미국에서 포닥으로 있던 연구실의 보스는 이론적, 실험적 측면에서 정교하고 심도 있게 유리를 연구하며 상당한 학문적 진전을 일군 유리 연구의 대가였다고 한다. 이 대가가 유리 제품으로 유명한 미국의 한 회사에서 세미나를 할 기회가 있었다. 유리 연구의 성과를 요약한 세미나를 다 끝낸 후 회사 관계자들에게 공동연구를 제안하니, 세미나에 참석한 회사 연구원 한 명이 이렇게 얘기했다고 한다. “교수님, 어떤 유리를 원하시는지요? 원하시는 유리의 성질만 말씀하시면 그게 뭐가 됐든 우리가 다 만들어 드리겠습니다.” 어느 정도나 정확한 얘기인지는 모르겠으나 이 일화는 유리를 학문적으로 연구하는 것과 유리를 실용적으로 다루고 응용하는 것이 생각만큼 직접적으로 연관되어 있지는 않음을 상징한다.
“유리의 재발견 [1]: 천의 얼굴을 가진 유리”에서는 유리가 기체, 액체, 고체와 같은 물질의 일반적 상태와 어떻게 다른지, 인류가 역사적으로 유리를 어떻게 활용해 왔는지에 대해 집중적으로 다뤘다. 아울러 현대 정보통신문명에서 유리 기술이 가지는 중요성에 대해서도 강조해 서술했다. 그러나 유리의 본성을 미시적인 관점에서 제대로 이해하려는 과학자들의 분투는 아직 명확한 승리를 거두지 못했다. 과학자들의 유리 연구는 현재 진행형이다. 즉, 동일한 구조를 가진 유리와 액체가 왜 그렇게 다르게 행동하는지에 대해 과학자들은 아직도 충분히 이해하지 못하고 있다. 이번 글에서는 액체가 유리 상전이 과정을 거쳐 유리로 변하는 과정에 대해 과학자들이 어느 정도나 이해하고 있고 어떤 관점으로 바라보고 있는지에 대해 다루고자 한다.[1-3] 즉 유리에 대한 학문적 관점과 호기심이 본 글의 주제다.
1. 유리 연구가 골치 아픈 이유
이상해도 너무 이상한 유리 상전이
액체를 급랭 시켜 유리로 변하는 과정을 보면 흡사 물질의 상phase이 변하는 것처럼 보인다. 자유롭게 흘러 다니는 액체가 고체처럼 딱딱한 물질(유리)로 변하는 것이니 이를 상의 변화라 생각해도 큰 무리가 없을 것 같다. 그러나 유리의 내부를 잘 들여다보면 문제가 그렇게 간단하지 않음을 알 수 있다. 이를 위해서 우선 중고등학교 과학 시간에 배웠던 상의 변화, 즉 상전이phase transition에 대해 잠깐 살펴보자.
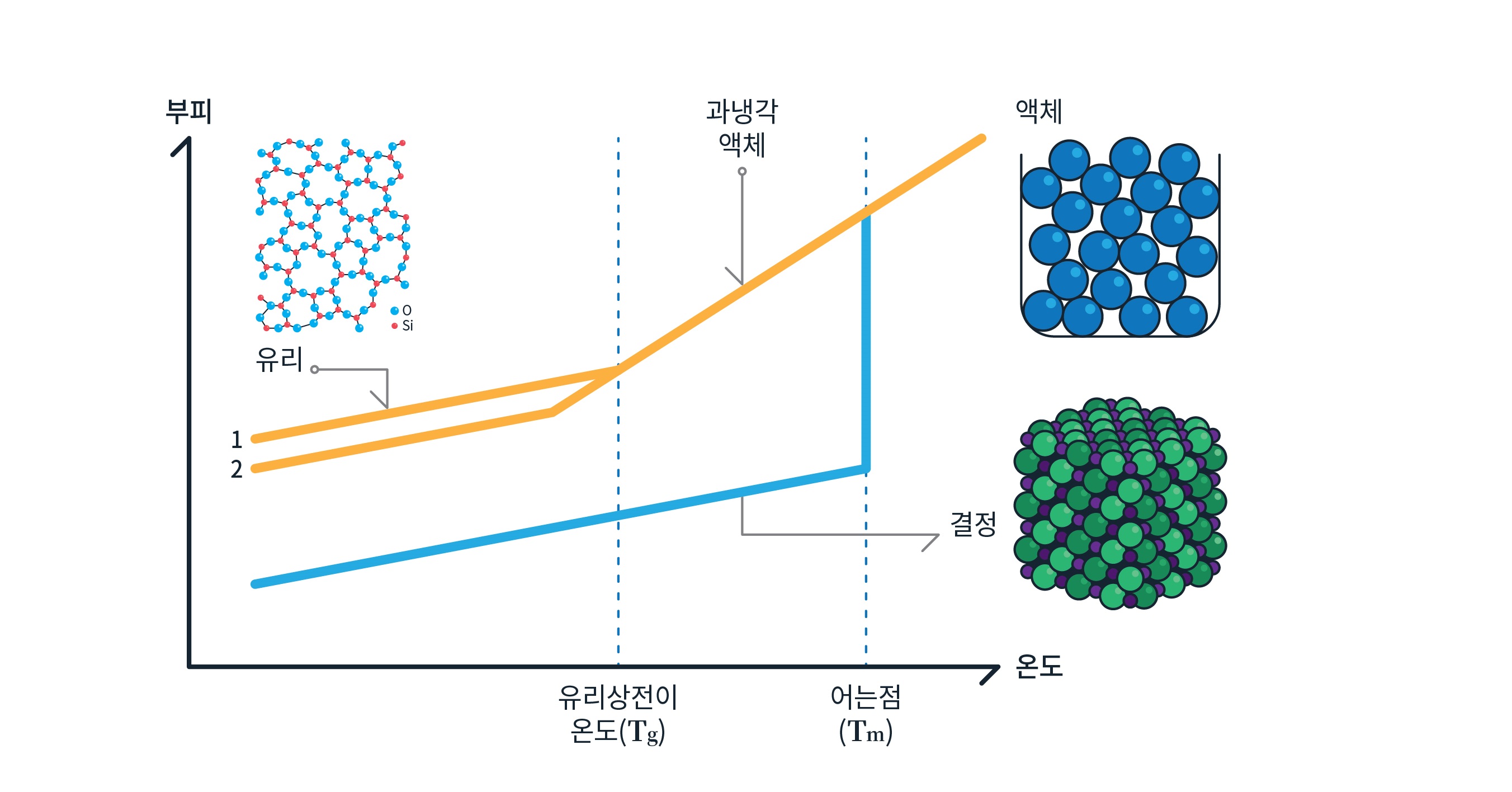
보통 물질의 상태를 기체, 액체, 고체로 나눈 후, 온도를 올리면 고체에서 액체, 액체에서 기체로 물질의 상태가 변하고 온도를 다시 낮추면 이 과정이 가역적으로, 즉 기체→액체→고체의 순서로 상전이가 일어난다고 배운다. [그림1]은 온도 변화에 따른 물질의 부피 변화를 보여준다.
고온에서 액체인 물질을 냉각시키면 부피는 점차 줄어든다. 온도에 따른 부피의 변화율을 나타내는 그래프상의 기울기는 액체의 열팽창 계수thermal expansion coefficient, 즉 온도를 1도 변화시켰을 때 부피가 변하는 정도를 보여주는 계수와 관련된다. 그러다가 해당 물질의 어는점Tm에 도달하면 액체에서 고체(결정)로 상전이를 하며 [그림1] 속 그래프처럼 부피가 불연속적으로 줄어든다. 결정으로 변한 물질을 더 냉각시키면 부피가 완만히 감소하고 이 기울기 역시 해당 결정(고체)의 열팽창계수를 반영한다. 고체는 일반적으로 액체보다 열팽창계수가 작다. 따라서 결정 상태의 부피 기울기가 더 완만함을 알 수 있다.
이처럼 상의 변화에 대해 과학 시간에 배운 지식으로는 일반적으로 모든 물질이 온도 변화에 따라 기체-액체-고체 사이에 상전이를 나타낼 것이라 예상할 것이다.1 [그림1]처럼 물질의 상이 바뀔 때 밀도가 불연속적으로 변하기 때문에 밀도를 측정함으로써 기체에서 액체, 혹은 액체에서 고체로 상이 변했는지 알 수 있다. 이처럼 물질의 상이 바뀔 때는 뚜렷이 변하는 물리적 성질로부터 해당 상전이의 질서 변수order parameter를 정의한다. 질서 변수는 온도나 압력의 변화에 의해 유도되는 물질의 상 변화에 관련되어 새롭게 나타나거나 사라지는 물성을 말한다.
상전이에 대해 조금 더 감을 갖기 위해 다른 예를 들어보자. 과학 실험의 단골 교구인 영구자석은 이름에 ‘영구’란 말이 붙어 있어서 자석의 성질(즉 자성)이 영원히 유지된다고 생각하기 쉽다. 그러나 자석의 온도를 올리면 영구자석의 성질이 사라진다. 자석의 흔한 재료인 철은 온도가 섭씨 약 770도를 넘어서면 자성을 잃어버린다.
“자석의 재발견: 양자역학에서 기억소자까지”에서 소개되었던, 자성의 미시적 원인인 스핀의 정렬 상태가 고온에서는 높은 열에너지에 의해 무너지는 것이다. 이 경우에도 자석에 자성을 부여하는 스핀의 정렬 정도를 나타내는 물성이 있고 이것이 자석으로의 상전이에 있어 질서 변수의 역할을 한다.2 스핀을 화살표로 비유하자면 화살표들이 한 방향으로 완벽히 정렬된 상태는 질서 변수의 값이 매우 높은 것이고 화살표들이 임의의 방향으로 무작위적으로 배열되어 있다면 질서 변수의 값은 0이 된다. 철이 자성을 띠기 시작하는 상전이 온도에서 이 질서 변수가 0에서 벗어나기 시작하는 것이다.
이제 다시 유리의 상전이로 돌아가 보자. 액체가 유리로 변하는 과정은 흔히 유리 상전이라 불리지만 그것이 일반적인 물질의 상전이와는 어떻게 다른지, 과연 상전이라 부를 수 있는지 생각해 볼 필요가 있다. 전술한 대로 액체의 온도를 급히 내리면 냉각 속도에 따라 액체는 어는점에서 결정으로 상전이가 일어나거나 소위 ‘과냉각 액체supercooled liquid’라 불리는 상태로 바뀐다. 냉각속도가 충분히 높다면, 즉 결정으로 성장할 수 있는 핵이 형성될 틈을 주지 않을 정도로 액체를 빨리 식히면, 물질은 결정으로의 상전이를 회피하며 액체와 비슷한 상태에 머무는 경향이 있다. 과냉각 액체는 구조적으로는 액체와 거의 동일하나 밀도가 약간 높고 점성이 높다는 점이 다르다.
과냉각 액체 상태에 놓인 물질의 온도를 더 낮춘다면 어떻게 될까? [그림1]에서 보이는 것처럼 흔히 ‘유리 상전이 온도(Tg)‘라 부르는 온도에서 온도-부피 기울기가 크게 변하며 유리상으로 넘어간다. 이 온도는 냉각속도에 따라 다소 달라지고 천천히 냉각할수록 더 낮은 온도에서 Tg가 나타난다. [그림1]에 표시된 1번과 2번 그래프로 설명한다면, 1번은 과냉각 액체를 다소 급하게 내린 것이고 2번은 천천히 냉각시킨 상태를 표현한다.
유리 상전이 온도에 대한 완벽한 정의는 아직 없지만 [그림1]에서 온도에 따른 부피의 기울기에 급격한 변화가 일어나는 온도에서 과냉각 액체의 점도viscosity가 약 1013 poise에 도달하는 것으로 알려져 있다.3 Tg에서 부피나 열팽창계수에 큰 변화가 나타나는 것은 Tg 이하에서 과냉각 액체가 변한 유리는 액체로서의 유동성이 실질적으로 사라지기 때문이다. Tg보다 낮은 온도에서 유리는 사실상 고체라 불러도 무방할 정도의 강도를 가진다. 이 그림의 저온에서 결정 상태의 물질과 유리 상태의 물질이 보여주는 부피의 기울기가 비슷하다는 것은 강도의 측면에서 두 물질의 상태가 매우 유사함을 보여준다. 우리가 유리를 건축 자재를 포함한 각종 산업 분야에 사용할 수 있는 이유가 이 때문이다.
그러나 유리 상전이 과정을 위에 설명한 다른 상전이처럼 생각하기는 쉽지 않다. 우선 일반적인 상전이는 상이 변하는 온도를 특정할 수 있으나(가령 물은 섭씨 0도에서 얼음으로 변한다), 유리 상전이 온도는 일률적으로 정해지지 않고 냉각 속도에 따라 달라진다. 결정은 원자들의 배치가 규칙적으로 일률적으로 결정되지만 무질서한 유리가 취할 수 있는 무작위적 구조의 수는 천문학적으로 많다. 게다가 유리 상전이 과정에서 유리를 액체와 구분할 수 있는 질서 변수가 무엇인지 확실치 않다. 유리는 과냉각 액체, 그리고 액체와 구조적인 면에서 별로 다르지 않기 때문이다. 즉 대칭성의 면에서 유리는 (과냉각) 액체와 동일하다.
에너지 산봉우리 속에서 헤매기
결국 액체가 과냉각 액체를 거쳐 유리로 변하는 과정은 아직도 일반적인 상의 변화에 비해서 명쾌히 이해되지 않고 있다. 액체가 결정(고체)으로 바뀌는 과정은 온도의 변화에 따라 해당 물질이 열역학적으로 더 안정된 상태로 바뀌는 것이다. 자연은 에너지의 관점에서 항상 안정한 상태, 더 낮은 에너지 상태를 선호하는 경향이 있다.
예를 들어, 수소 원자 두 개가 붙어서 하나의 수소 분자를 형성하는 것은 수소 원자 두 개(가 서로 매우 멀리 떨어져 있을 때)의 에너지의 합에 비해 수소 분자 하나의 에너지가 더 낮아서 수소 분자가 더 안정된 상태에 놓일 수 있기 때문이다. 물질의 상전이도 비슷하다. 액체가 결정될 때 원자나 분자들이 배열될 안정적인 주기적 구조는 일반적으로 한 종류다. 따라서 냉각되는 액체가 가야 할 선택지는 딱 하나다. 열역학적으로 더 안정한 규칙적인 배열의 결정 구조다. 마찬가지로 고온에서 제멋대로인 스핀의 방향이 특정 온도에서 한 방향으로 정렬하며 자성을 띠는 것도 저온에서 스핀이 정렬한 상태가 더 안정적이기 때문이다.
이런 접근법을 유리 상전이 과정에 적용하면 어떻게 될까? 액체가 과냉각 액체를 거쳐 유리상으로 변할 때 원자나 분자들이 배치될 수 있는 구조는 결정과는 다르게 무작위적이고 무질서하기 때문에 허용되는 구조의 수는 천문학적으로 클 것이다. 아보가드로 숫자 정도의 입자들을 일정한 공간에 마구잡이로 배치할 경우의 수를 상상해 보라.4
비유하자면 운동장에서 정사각형 대열로 똑바로 정렬해 있는 군인의 경우에 비해 마구잡이로 여기저기 뛰어 돌아다니는 초등학생들의 무작위적 배열 상태는 엄청나게 많을 것이다. 게다가 충분히 오랜 시간을 기다리면 학생들의 끊임없는 움직임으로 인해 허용되는 모든 배열 상태가 눈앞에 순차적으로 펼쳐질 것이다. 액체의 경우도 마찬가지다. 충분한 시간 동안 기다리고 관찰하면, 액체 속 분자들의 끊임없는 열적 움직임으로 인해 허용된 모든 무작위적인 구성, 무작위적인 원자 배치 사이를 해당 계가 끊임없이 계속 왔다 갔다 할 수 있다.
반면에 급랭시킨 액체가 결정화를 피하고 과냉각 액체로 변할 경우에는 점성이 커지면서 한 원자/분자의 움직임이 주변의 원자/분자의 흐름에 방해받으며 동적인 활력이 떨어진다. 결국 냉각 과정에서 유리 상전이 온도를 지나면서 그 무수히 많은 가능한 배치 중 단 하나로 고정되어서 결국 거기에 그대로 갇혀 버린다. 비록 거기가 열역학적으로 가장 안정한 상태가 아님에도 불구하고 말이다. 이런 유리의 상태를 열역학적으로 준안정metastable 상태라고 부른다. 게다가 냉각을 통해 도달하는 유리상의 무질서한 구조는 냉각 속도나 열적 처리 방법에 따라 달라진다. [그림1]을 보면 더 천천히 냉각시킨 과냉각 액체의 유리 상전이 온도가 더 낮고 부피도 더 작은 것을 알 수 있다. 이는 과냉각 액체를 더 천천히 냉각했을 때 유리의 가능한 다양한 배열 중 구조적으로 더 치밀한 배열의 유리상으로 변하면서 부피가 조금 더 줄어든다는 것을 보여준다.
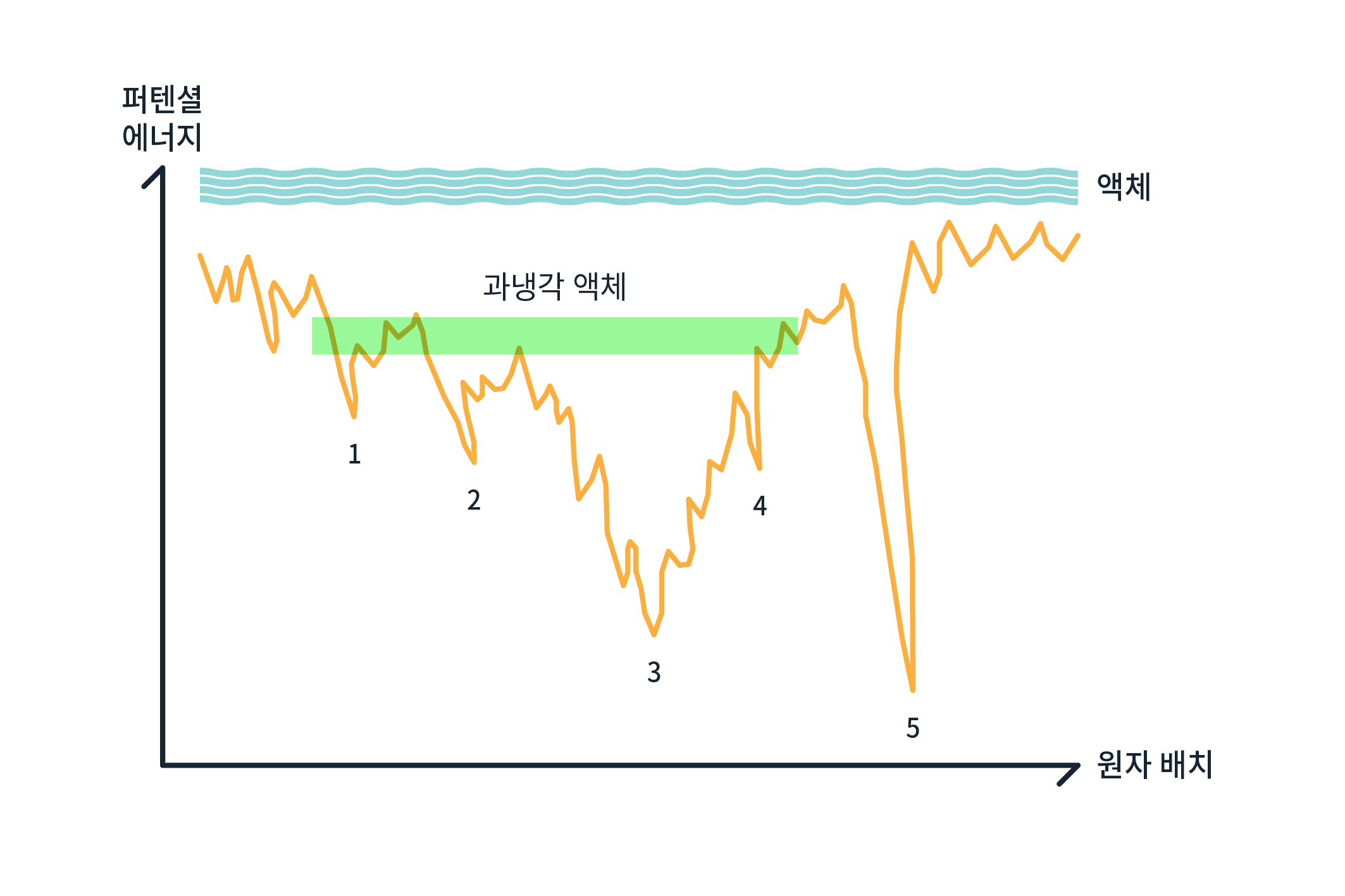
이처럼 액체가 과냉각 액체에서 유리로 도달하는 상태는 보통 [그림2]와 같은 에너지 전경energy landscape이라 부르는 도표를 이용해 개념적으로 나타낸다. [그림2]의 가로축은 원자들의 가능한 모든 배치를 나타낸다. 원자의 배치가 결정되면 우리는 이 배치에 따르는 퍼텐셜(위치) 에너지를 구할 수 있다. 이를 세로로 표현했다. 따라서 이 그림은 허용되는 원자/분자의 배치에 대해 에너지를 평가한 일종의 채점표 같은 것이다. 세로축의 에너지는 열역학적으로 좀 더 엄밀한 의미에서 정의가 필요한 함수지만 여기서는 에너지가 낮을수록 해당 계가 더 안정적인 상태라 생각하는 걸로 충분할 것 같다. 평형 상태의 액체는 그림처럼 당연히 에너지가 높고 그림에서 제시된 모든 원자/분자의 배치 중 하나를 취할 수 있다(사실 이 배열들 사이를 끊임없이 왔다 갔다 하는 중이다). 액체가 냉각되어 과냉각 액체 상태가 되면 계는 과냉각 액체가 가지는 에너지보다 더 높은 에너지의 상태를 취하진 못할 것이다. 반면에 자신보다 더 낮은 에너지를 가진 배열 중 하나를 취할 수 있다.
액체에서 결정으로 상전이 하는 물질은 이 그림에서 어디에 위치할까? 위에서 설명했듯이 상전이 온도 이하에서 결정은 해당 물질의 가장 안정적인 상태가 된다. 따라서 그림에서 에너지가 가장 낮은 5번 위치가 바로 결정 상태에 대응한다. 그러나 유리 상전이를 하는 물질의 경우에는 온도가 낮아짐에 따라 다양한 극소점에 자리를 잡고 거기서 버틸 가능성이 높다. 가령 1, 2, 3, 혹은 4번 상태 중 하나에 갇힐 것이다. 이 다양한 극소점들 하나하나가 모두 유리의 서로 다른 구조적 배치나 상태를 표현한다.
냉각 과정 중 이 극소점 중 하나에 갇히면 에너지 장벽이 그리 높지 않은 이웃의 극소점으로 이동하는 것은 가능하지만 상당히 높은 에너지 장벽을 넘어 다른 구조로 가는 것은 실질적으로 불가능해진다. 게다가 운 좋게도 결정 상태 근처의 극소점에 자리 잡고 결정 상태로 넘어가는 에너지 장벽이 높지 않은 경우에는 결정으로 안착할 수도 있다. 실제로 과냉각 액체 상태에서 온도를 고정하고 한참 기다리면 결정으로 바뀌는 물질들도 존재한다. 그러나 일반적으로 저온의 유리상에서는 원자와 분자가 더 안정한 상태를 향해 움직이며 구조를 바꿀 수 있는 열적 에너지가 충분하지 않아 열역학적으로 더 안정한 결정의 상태로 변화되지 못한다.
이런 과정을 첩첩산중 속에서 헤매는 등산으로 비유해 보자. 정상을 찍은 후 사방으로 둘러싸인 산봉우리 사이로 정신없이 내려오는 과정은 중력 위치 에너지의 입장에선 안정적인 곳을 찾아가는 과정이다. 엄청나게 복잡한 산악 지형을 헤치며 오르내리는 과정에서 우연히 어느 골짜기에서 평지를 찾았다고 하자. 사방이 산으로 둘러싸인 그 안락한 평지에 머무르는 사람은 드디어 자신이 가장 안정적인 곳에 도착했다고 착각할 수 있다. 그러나 언덕을 몇 개 더 넘어야 지금 머무는 곳보다 더 낮은 진정한 평지에 도달할 수 있음을 그 사람은 모르고 있다. 이 등산가는 가장 안정적인 곳이 아닌 준 안정한metastable 곳에 머물러 있는 것이다. [그림2]는 자유 에너지라는 첩첩산중에서 냉각에 따라 낮은 에너지 상태를 찾아 헤매다가 결국 어느 국소적인 평지에 갇혀 유리로 굳혀진 물질의 운명을 잘 보여준다.
자연은 에너지가 낮은 상태를 선호한다고 했다. 그렇다면 절대온도 0도가 아닌 다음에야 열에너지가 있는 것이고 따라서 한참을 기다리면, 에너지가 준안정한 상태에서 가장 낮은 결정의 상태로 내려올 수 있을까? 주변에 에너지 장벽이 다소 낮은 곳을 넘어 인접한, 그러나 구조적으로 비슷한 상태로 옮겨가는 것은 아마 오랜 시간이 지나면 가능할 것이다. 실제로 유리상에서 어떤 특성을 측정할 때 그 특성이 시간에 따라 천천히 변하는 현상들이 보고됐다. 이를 에이징aging이라 부르는데, 복잡한 에너지 장벽의 구조 속에서 해당 물질이 조금 더 낮은 에너지 상태를 찾아 움직이는 특성이 반영된 것으로 해석한다.
그렇지만 가장 낮은 에너지 상태로 가는 중간에 매우 높은 에너지 장벽들이 가로막고 있다면 이를 넘어 이동하는 것은 우주의 나이만큼 기다려도 불가능할 것이다. 깊은 산속을 헤매며 에너지를 다 소진해 버린 등반가에게 눈앞에 버티는 거대한 언덕을 다시 올라 반대편으로 내려가는 것이 무리인 것처럼 말이다. 준 안정한 상태에 갇혀 열에너지의 도움도 받지 못하고 그 상태 그대로 얼어 버린 유리가 바로 첩첩산중에 둘러싸여 퍼질러 앉은 등반가의 좌절된 모습에 비유될 수 있을 듯싶다.
유리 상전이는 정말 상전이인가?
액체가 과냉각 액체를 거쳐 유리로 변하는 과정을 흔히 유리 ‘상전이’라 부르지만, 이것이 정말 상전이일까? 액체가 고체로 바뀌거나 자석이 아닌 상자성 상태에서 강자성 상태의 영구 자석으로 바뀌는 것과 비슷한 물리적 과정일까? 이것이 지난 반세기 동안 유리를 연구하는 과학자들을 괴롭혀 온 핵심적인 질문 중 하나다.
과냉각 액체 상태에서 여러 특성을 측정해 보면 과냉각 액체의 다양한 동적인 특성들, 이들이 나타내는 동적인 변화가 계속 느려지는 것을 알 수 있다. 이 글에서 유일하게 등장하는 수식 하나를 여기 소개한다.5
η(T) = AeB/(T-T0)
고등학교 때 배우는 지수함수로 표현된 이 식에서 η 는 우리가 측정하는 물리량으로 가령 점도viscosity 혹은 외부 자극에 대한 반응 시간과 같은 측정량이다. T는 온도이고 A, B, T0는 모두 상수다. 지수함수 ex에서 x가 커지면 함수의 값이 급격히 증가한다는 것을 기억할 것이다. 위 식의 지수함수에서 지수 부분인 Β/(Τ – Τ0)을 보면 온도 T가 T0보다 큰 영역에서 T0를 향해 가까이 갈수록 분모가 줄어드니 지수 부분은 급격히 늘어나다가 T=T0에서 무한대로 발산하게 된다. 따라서 지수함수가 나타내는 물성 역시 냉각에 따라 급격히 커지면서 발산하는 듯한 양상을 보인다.
예를 들어 액체에서 과냉각 액체를 거쳐 유리 상전이 온도에 도달하는 동안 점도는 수천 조 배 정도나 증가한다(수천 배가 아니라 수천 조(!) 배다). 이는 흡사 절대온도 0도가 아닌 특정 온도에서 거의 모든 동적 특성이 완벽히 동결, 냉각되는 것처럼 보임을 시사한다. 이런 과정은 유리를 구성하는 원자나 분자들이 (제자리에서 떠는 동작을 넘어) 열적 에너지의 도움으로 주위의 다소 비어 있는 곳으로 이동하려 할 때 이를 가로막는 에너지 장벽의 높이가 무한히 올라가 결국은 전혀 움직이지 못하는 상황으로 내몰린다고 볼 수 있다.6
이런 급격한 동적인 변화를 물질의 상이 변하는 상전이로 해석할 수 있을까? 액체가 유리로 바뀌는 과정에 대해 과학자들이 제안한 이론적 모델들을 단순화시키면 크게 두 가지 흐름으로 나누어진다. 하나는 유리로 변하는 과정이 그저 동적으로 한없이 느려지기만 하는 과정이라는 것이다. 이 견해는 흡사 영화를 상영할 때 상영 속도를 정상 재생 속도에서 시작해 0.1배, 0.01배, 0.001배… 등 재생 속도를 한없이 느리게 만들며 보는 동영상의 모습을 보는 것이라 비유해 볼 수 있다. 이런 경우에는 유리 상전이 과정에 특별히 흥미로운 물리를 기대하기는 쉽지 않다. 그저 결정에 다다르지 못한 무질서한 동결 상태만 존재할 뿐이다.
또 다른 관점은 유리 상전이 과정 역시 액체가 결정으로 변하는 상전이처럼 본질적으로 상이 바뀌는 성격을 가지고 있지만, 우리가 아직 그 과정을 제대로 이해할 만큼 똑똑하지 못하다는 것이다. 실제로 비열과 같은 열역학적 성질을 측정하면 유리 상전이 온도에서 특이한 변화를 보인다. 이것이 열역학적 분석이 가능한, 또 다른 상전이로 밝혀진다면 이건 과학자들에게 새로운 차원의 탐구 대상, 연구의 신천지가 열리는 셈이 될 것이다. 새로운 방식의 이론과 실험, 근본적인 사고의 전환을 요구하기 때문이다.
그렇다면 과학자들이 생각하는, 상전이를 경험한 이상적인 유리ideal glass의 모습은 무엇일까? 이에 대한 힌트는 [그림1]에서 얻을 수 있다. 과냉각 액체를 냉각시키는 속도를 줄임에 따라 유리 상전이 온도가 낮아지면서 부피가 더 작고 더 치밀한 유리, 더 안정적인 유리를 얻을 수 있다고 했다 (1번과 2번 그래프를 비교해 보자). 만약 결정화를 피하면서 과냉각 액체를 무한히 느린 속도로 냉각시킬 수 있다면 어떻게 될까?
아마도 냉각 과정에서 원자들의 배치가 더 안정적인 상태로 변하면서 [그림2]에서 3으로 표시된, 에너지가 가장 낮은 유리상에 안착할 것이다. 혹은 2번이나 4번의 위치에 있다 하더라도 무한히 긴 시간을 기다린다면 3번이라는 안정적인 상태를 향한 지난한 여행이 가능할 수도 있다. 이렇게 도달한 이상적인 유리 상태는 단 하나의 배치를 가진 가장 치밀하고 가장 안정적인 무질서 상태로 액체나 고체의 상과 비견될 수 있는 상태로 여겨져 왔다. 그러나 이런 이상적인 유리 상태에 도달하기 위해서는 무한히 느린 냉각 속도 혹은 무한히 긴 시간이 필요하기에 이상적인 유리를 연구하는 것은 난망한 것으로 간주하였다. 2절에서는 이상적인 유리를 찾아 나서는 과학자들의 고투와 최근의 성과가 간략히 그려진다.
2. 유리가 여는 새로운 과학과 기술
유리 연구의 확장
유리의 구조적 무질서, 느린 동역학적 거동, 시간에 따라 변하는 에이징 현상 등 유리의 복잡성은 그간 과학자들을 괴롭히며 유리에 대한 완벽한 이해를 방해했다. 난공불락처럼 보이는 적의 진지를 정공법으로 공격하는 것이 힘들면 우회 전술을 택하는 것도 한 방법이다. 지금까지 설명했던 유리들의 특징은 원자나 분자들의 배치가 무질서하고 구조적 규칙성이 없다는 것이었다. 이런 면에서 이들을 구조 유리structural glass라 부른다. 재밌게도 이런 구조 유리의 특성은 우리에게 친숙한 산화물 유리에서만 보이는 건 아니다. 고분자에 기반한 비정질 물질, 다양한 바이오 물질, 음식 등 유리 상의 특징을 보이는 물질들은 무척 풍부하다. 과학자들의 유리에 대한 연구의 궁극적 목적은 이처럼 다양한 형태와 구조, 조성을 보이는 유리 물질들의 보편적 특성을 파악하고 이를 설명할 수 있는 이론을 구축하는 것이다.
그런데 유리 연구에 있어서 과학자들이 선택한 방법 중 하나는 구조적인 무질서를 띠는 구조 유리보다 조금 더 단순하지만, 유리의 보편적 특성을 가진 물질들을 찾아서 연구하는 것이다. 구조 유리의 경우 유리의 구성단위(원자나 분자)가 위치 및 방향의 측면에서 모두 무질서하다. 만약 구성단위의 위치는 규칙적이지만 방향만 무질서하다면 이해하기가 조금 더 쉽지 않을까?
가령 결정처럼 원자들이 주기적으로 배열해 있는 물질임에도 불구하고 유리상과 비슷한 성질을 보이는 시스템들이 있다. 가장 대표적인 예가 1970년대부터 매우 활발하게 연구되어 온 스핀 유리spin glass다.[6] 스핀 유리란 자성체 중 스핀의 방향이 제멋대로 무질서한 상태를 보이다가 냉각됨에 따라 저온에서 그대로 동결해 버리는 상태를 말한다. [그림3]을 보면 스핀들이 한 방향으로 정렬해 있는 강자성체(자석)와 스핀의 방향이 무작위적으로 배열된 스핀 유리가 비교되어 있다.
비슷한 방식으로 유리상을 구현하는 또 다른 시스템으로는 (전기) 쌍극자 유리dipole glass를 들 수 있다. 여기서 전기 쌍극자란 결정을 이루는 내부 구성단위에서 양전하(+)의 중심과 음전하(–)의 중심이 어긋나 있는 경우를 가리킨다. 이 쌍극자가 결정의 내부에 생기는 경우 결정의 주기성에 부합되게 쌍극자 역시 주기적으로 위치하고 이를 스핀과 비슷하게 화살표로 표시할 수 있다. 가령 음전하의 중심에서 양전하의 중심으로 화살표를 그리면 결정 내 각 지점에 자리한 쌍극자의 방향을 표시할 수 있다. 고온에서는 결정 내 쌍극자들의 방향이 제멋대로 마구잡이로 움직이다가 온도를 낮추면 내부의 상호작용에 따라 몇 가지 가능성이 생긴다.
우선 특정 온도에서 모든 쌍극자가 동일한 방향으로 정렬하는 상전이가 발생할 수 있다. 이런 물질을 강유전체ferroelectrics 라 부르고 비휘발성 메모리나 압전 소자 등 다양한 분야에서 활용되고 있다. 반면에 어떤 물질의 경우에는 온도를 낮추게 되면 쌍극자의 방향이 무작위적이고 제멋대로 놓인 배열 그대로 동결되어 버린다. 이를 쌍극자 유리라 부른다. 스핀 유리든 쌍극자 유리든 결정의 주기성은 유지가 되고 있지만, 그 위에 덧씌워져 있는 스핀과 쌍극자의 방향이 무질서하게 배열되어 있고 그것이 저온에서 그대로 동결된다는 특징을 가지는데 이런 동결된 무질서가 구조 유리와 비슷한 측면이라 할 수 있다.
이들은 구조적으로는 결정의 주기성을 가지고 있는데도 어떻게 유리와 비슷한 특성을 띨 수 있는 것일까? 자기 스핀이나 전기 쌍극자의 방향이 무질서한 상태로 얼어버리기 위해서는 두 가지 핵심적인 요소가 필요하다. 하나는 스핀이나 쌍극자를 같은 방향으로 정렬시키는 힘과 이들을 서로 반대 방향으로 정렬시키기 위한 힘이 공존하며 서로 경쟁해야 한다. 자성체의 경우 전자를 강자성 상호작용ferromagnetic(FM) interaction, 후자를 반강자성 상호작용antiferromagnetic(AFM) interaction이라 부른다. 후자의 경우 한 스핀이 위를 향하면 이웃한 스핀은 거꾸로 뒤집혀 아래를 향해야 한다. 게다가 이 두 가지 상호작용이 결정 내에 무작위적으로 배치되어야 한다.7
이런 상황이 유리의 특성을 어떻게 만들어 내는지 [그림4]를 보면서 이해해 보자. 여기서는 2차원의 사각 격자 구조 위에 스핀이 위 혹은 아래만 향할 수 있다고 가정한다. 스핀과 스핀 사이의 상호작용은 강자성FM 혹은 반강자성AFM으로 표기되어 있다. [그림4]의 왼쪽은 강자성 물질로서 모든 스핀 사이의 상호작용이 FM이라 스핀을 나타내는 화살표들이 동일한 방향(여기서는 위)을 향한다. 이제 오른쪽의 스핀 유리의 경우를 보자. 이 경우는 스핀과 스핀 사이의 상호작용으로 FM 혹은 AFM이 위치별로 무작위적으로 배정된다.
[그림4]의 예를 보면 FM과 AFM의 상호작용에 따라 왼쪽 위, 오른쪽 위, 왼쪽 아래의 스핀이 정렬되어 있음을 알 수 있다. 그런데 오른쪽 아래 물음표가 붙어 있는 격자점을 보면 이곳의 스핀은 그 위의 스핀과의 FM 상호작용을 만족하기 위해선 위로 정렬해야 하나 왼쪽 스핀과의 FM 상호작용을 만족하기 위해선 아래로 정렬해야만 한다. 즉 스핀이 어느 방향이든 양쪽의 상호작용을 동시에 만족하는 건 불가능하다. 이런 상황을 스핀의 좌절frustration이라 부른다. 다른 맥락에서 본다면 이 위치의 스핀이 위를 향하든 아래를 향하든 에너지는 동일하다는 것이다.
스핀 유리 내 격자점의 수는 아보가드로 숫자 정도 있고, 그 속에 무작위적으로 경쟁하는 두 상호작용을 만족하지 못하는 스핀들은 좌절을 경험하며 다양한 에너지 상태를 나타내는 엄청나게 많은 무작위적인 상태들을 보일 것이며, 냉각됨에 따라 그중 하나로 고착되어 동결된다. 천문학적인 수의 스핀들의 배열 방식에 따라 펼쳐지는 에너지의 분포는 흡사 [그림2]에서 보여줬던 에너지 전경과 비슷할 것이다. 냉각하게 되면 각각의 스핀은 자기 주위에서 요구하는 상호작용들을 가능한 최대로 만족시키려 하면서 낮은 에너지 상태를 찾아 움직이겠지만 저온에서 열적 에너지의 부족으로 인해 결국 하나의 무작위적인 스핀 배열을 가진 상태로 동결되어 버린다. 이는 에너지 전경 내 국소적인 에너지 우물에 갇혀 빠져나오지 못하는 상황에 내몰리는 것이다. 그렇게 스핀의 움직임은 동역학적으로 느려지는 과정이 될 것이고 이 과정은 구조 유리와 매우 비슷한 특징들을 공유하고 있다.
결정 구조 속에서 주기적으로 배치된 원자나 분자에 부여되는 다른 특성들, 즉 자성체의 스핀, 전기 쌍극자, 혹은 분자의 방향 등이 무질서한 상태로 동결되는 이런 계들 역시 구조 유리와 매우 비슷한 동역학적인 특성을 나타낸다. 이런 독특한 유리들의 동역학적 성질은 어떤 방법으로 조사할 수 있을까? 외부에서 살짝 자극을 주고 그 반응을 살펴보는 것이 대표적이다. 스핀의 경우 외부에서 자기장의 방향이 주기적으로 변하는 교류 자기장을 가하면서 스핀이 그 변화를 어떻게 따라오는지 확인한다. 외부 자기장이 천천히 변하면 스핀은 그 변화를 잘 따라가다가 자기장의 변화를 빠르게 하면, 즉 교류 자기장의 주파수를 높이면 스핀이 그 변화를 따라가지 못하는 특성 주파수가 확인된다. 이 주파수의 역수가 바로 해당 스핀 시스템의 반응 시간에 해당한다. 마찬가지로 전기 쌍극자 유리의 경우에는 주기적으로 변하는 교류 전기장을 걸어서 반응 시간을 확인할 수 있다.
이 글에서 소개한 유일한 식이 하나 있었다. 그 식에서 η는 구조 유리의 점도를 나타내는 것으로 해석했었다. 그런데 스핀 유리와 쌍극자 유리에서는 이 η를 위에서 소개한 반응 시간으로 바꾸어도 그대로 성립한다. 즉 물질 속 스핀이나 쌍극자가 외부의 주기적인 변화에 대해 반응하는 시간이 온도를 낮추면 점점 증가하다가 특정 온도에서 발산하는 듯한 동역학적 특성을 보이는 것이다. 물론 실험실에서 수행할 수 있는 실험의 주파수는 아무리 낮아도 1,000분의 1Hz나 마이크로 Hz 정도이기 때문에 반응 시간의 발산을 직접 확인할 수는 없다. 그러나 반응 시간의 온도 의존성이 상당히 넓은 온도 영역에서 이 식을 만족한다는 것은 저온의 특정 온도에서 스핀이나 쌍극자와 같은 자유도가 완벽히 동결하는 특이성을 가질 수 있다는 점을 시사한다.
스핀 유리와 같은 무질서계에 대한 이론적 탐색은 1970년대부터 매우 활발히 진행되기 시작했다. 이런 과정에서 보통 스핀과 스핀 사이의 상호작용을 가장 가까운 거리로 국한하거나 무한대의 거리까지 가정하는 등 단순한 가정을 활용함으로써 어느 정도 정교한 이론적 모델들이 만들어졌다. 그러나 스핀 유리 및 쌍극자 유리 등의 모델과 구조 유리 사이의 유사성 및 스핀 유리에 대한 매우 정교하고 광범위한 이론적 성취에도 불구하고 이런 이론이 구조 유리에서 나타나는 동역학적 특성, 가령 유리 상전이 온도 아래에서 예측되는 점도의 발산 등을 설명하는 데 활용될 수 있는지에 대해서는 의견이 분분하다.[1]
유리에 대한 심화된 이해를 위해
앞서 살펴본 1절 “유리 연구가 골치 아픈 이유는”에서는 ‘이상적인 유리’에 대한 설명으로 끝을 맺었다. 도달하기 힘든 냉각 속도나 대기 시간으로 인해 이상적인 유리를 직접 구현하는 것은 불가능하다. 놀랍게도 과학자들은 난제에 부딪히면 항상 우회로를 개척한다. 하나는 컴퓨터 시뮬레이션이다. 최근 계산 알고리즘의 개선으로 매우 느린 냉각속도를 거친 유리를 구현하는 것이 가능해졌다.[7]
다른 하나는 바로 초에이징Superaging된 유리, 즉 수천만 년 동안 방치된 유리에 관한 연구이다.[8] 설명한 것처럼 유리는 끊임없이 가장 안정적인 평형 상태를 향해 나아가려는 비평형 계로 볼 수 있어서 시간이 지남에 따라 특성이 변하는 성질을 가지고 있다. 이는 기본적으로 유리를 이루는 분자들이 더 안정된 상태를 찾아 끊임없이 움직이고 자신을 재배치하려는 동적인 특성과 관련된다. 그러나 유리 상전이 온도보다 훨씬 낮은 온도에서 에이징이 진행되는 속도는 엄청나게 느리다. 과학자들은 가령 수천만 년 된 호박amber 유리를 조사함으로써 이상적인 유리 상태에 대한 간접적 지표로 사용한다.
마지막으로, 인공적인 방법으로 이상적인 유리 상태를 구현해 보려는 움직임이 있다. 2007년 저널 사이언스에는 매우 흥미로운 논문이 한 편 실렸다.[9] 소위 물리 기상 증착법physical vapor deposition, PVD을 통해 고밀도 박막 유리의 구현이 가능하다는 논문이었다. 이 논문에서는 기판의 온도를 유리 상전이 온도보다 50도 낮게 유지한 상태에서 유기 물질들을 매우 높은 밀도로 유리상으로 증착할 수 있음을 보였다. 이는 주로 유리의 자유로운 표면 위에서 분자들의 이동도가 물질 내부보다 십억 배나 높기 때문으로 해석되었다. 즉, 비록 유리상 전이 온도보다 낮은 온도 조건임에도 불구하고 표면 근처 분자들이 높은 이동도로 인해 짧은 시간 동안 자신들을 재배치하며 보다 치밀한 구조의 유리로 탈바꿈하는 것이다. 이 기법을 통해 탄생한 유리는 같은 재료의 일반적인 유리보다 15% 정도 더 밀도가 높은 것으로 보고되었다.
이런 방법을 통해 간접적으로 구현된 ‘이상적 유리’ 상태에 대해 과학자들은 무엇을 하고 싶은 것일까? 당연히 우리가 주위에서 흔히 볼 수 있는 이상적인 유리와 무엇이 같고 무엇이 다른지 비교해 보는 것이 우선이다. [그림2]의 다양한 극소점 중 하나에 갇혀 버린 유리는 에너지가 조금 더 낮은 주변의 극소점으로 탈출하기 위해 끊임없이 노력한다. 거의 동일한 에너지를 가진 상태들이 매우 많기 때문에 계가 비슷한 상태들 사이를 왔다 갔다 하는 것은 충분히 가능하다. 이런 과정은 1K 정도의 저온에서는 소위 양자역학적 터널링 현상을 통해 이루어지는데 이를 비열 측정을 통해 확인할 수 있다.8
반면에 이상적인 유리는 이미 가장 안정적인 상태에 도달해 있어 다른 상태로 옮겨갈 여지가 없다. 재미있게도 컴퓨터상에서 구현된 이상적 유리, PVD를 통해 구현된 박막 유리에서는 터널링 현상에 기인한 비열이 확인되지 않거나 매우 미약한 반면에 4천만 년을 넘는 시간 동안 자연에서 버텼던 호박 유리는 일반적인 유리와 동일하게 터널링 현상에 의한 비열이 확인되었다고 한다.[7,10,11] 이런 결과는 이상적인 유리 상태가 존재할 수 없다는 간접적 증거인가? 호박 유리는 오랜 시간 동안 자연스럽게 많은 불순물을 함유하게 되어 이상적인 유리로 간주할 수 없는 것인가? 이런 질문들에 대답하기 위한 과학자들의 최신 결과들은 유리에 대한 연구가 현재진행형일 뿐만 아니라 앞으로 더욱 활발하게 진행될 것이라는 점을 시사한다.
유리 응용의 재발견
유리에 대한 이론적 접근과 함께 새로운 방법으로 새로운 조건이나 특성의 유리를 만들려는 노력도 치열하게 벌어지고 있다. 최근 30-40년 동안 새로운 조성의 유리가 개발되면서 그 종류가 급증하고 있고 현재 시판되고 있는 유리의 종류는 대략 천 종 이상이라 한다. 게다가 잘 알려져 있던 유리라도 이를 손쉽게 사용할 수 있는 제조 공정에 대한 연구도 활발하다. 가령 녹는점이 높아 가공하기가 매우 까다로운 용융 실리카fused silica 유리를 손쉽게 가공해 3차원 프린팅의 재료로 활용하는 기법 등이 최근 발표된 바 있다.[12]
1편의 글에서 현대에 유리를 가공하는 기술 및 유리가 응용되는 분야에 대해 개략적으로 설명했지만, 유리의 진화는 오늘날에도 끊임없이 이루어지고 있다. 가령 충격에 강한 강화 유리는 이제 디스플레이의 얼굴이 된 지 오래다. 최근 폴더블foldable 스마트폰이 등장하면서 플렉서블 디스플레이에 사용될 수 있는 구부러지는 유리에 관한 연구나 수요도 강해지고 있다. 국내 한 대기업이 2020년 초 출시한 폴더블폰에 적용된 초박막 유리ultrathin glass가 아마 최초의 적용 사례일 것 같다. 두꺼운 유리를 휘면 가장 바깥에 위치한 원자들에 미치는 응력이 강해져 쉽게 깨지지만, 유리를 수십 마이크로미터 정도로 얇게 가공할 경우 바깥층 원자에 가해지는 응력이 약해지며 높은 곡률로 유리를 휠 수 있다. 이런 초박막 유리를 얼굴로 삼은 차세대 플렉서블 디스플레이의 대중화가 곧 일어나리라는 예상이 많다.
보통 수분이나 산소에 오래 노출되는 유리 중 일부는 조성에 따라 부분적으로 결정화가 일어나는 경우도 있지만, 대부분의 유리의 안정성은 놀랄 정도로 높다. 자연에서 발견되는 천연 유리 중에는 수백만 혹은 수천만 년의 나이를 가진 것들도 있고, 아폴로 15호를 타고 달에 간 우주인들이 가져온 유리 샘플의 경우 무려 30억 년이나 지났지만 지금도 안정적인 유리 상태를 유지하고 있다고 한다. 내열성, 내화학성, 내부식성 등의 장기 안정성으로 인해 유리는 음식 등 오랜 기간 동안 다양한 물질의 저장 용기로 활용됐다. 이런 유리의 안정성을 이용하면 오랜 기간 분리해 저장해야 하는 핵폐기물을 가두는 용기로도 활용할 수 있다. 특히 재처리 과정에서 나오는 고준위 방사능 쓰레기를 실리카 기반 유리와 함께 고형화하는 기술에 대한 연구가 활발하다.[13]
활발히 연구되고 있는 또 다른 분야는 금속 유리metallic glass다.[14] 일반적인 유리는 원자들의 위치도 무작위적이고 원자들 사이의 결합 방향도 제멋대로라서 유리로 만들기가 상대적으로 쉽다. 그런데 자유 전자의 집단적 공유로 형성되는 금속 결합의 경우 결합의 방향성이 없어서 금속을 이루는 원자들은 쉽게 결정을 이룬다. 이로 인해 금속 원자들이 무작위적으로 배열된 금속 유리를 만드는 것은 매우 힘들었다. 1950년대 초당 1조 도의 냉각 속도로 비정질 금속을 만드는 데 성공한 이래 요즘은 적절한 조성의 금속 합금에 대해 초당 백만 도 혹은 천 도 정도의 냉각 속도로도 금속 유리를 만들 수 있을 정도가 되었다. 금속 유리는 금속 결정에 존재하는 결함들도 없어서 공학적으로 매우 강한 재료로 활용될 수 있어 지금도 많은 연구가 이루어지고 있다.
유리는 사람들이 생각하기 힘든 의외의 분야에서도 매우 중요한 역할을 하는 재료다. 흔히 유기발광다이오드Organic Light Emitting Diode, OLED라 부르는 디스플레이에서 발광층의 역할을 하는 유기층 속의 유기 분자들 역시 유리처럼 무질서한 배치의 성격을 가진다. 최근 이들 유기 분자의 방향을 액정처럼 한 방향으로 나란하게 배치함으로써 OLED의 발광 효율을 크게 개선한 연구 결과들이 발표되고 있다. 아스피린과 같은 약제 물질은 체내에 들어갔을 때 빠른 흡수율이 중요하다.
약제 물질을 결정으로 제조하지 않고 유리 상태로 제조할 경우 체내 흡수율이 증가한다는 결과들이 보고되면서 약제물질의 유리 상전이 과정에 대해서도 최근 활발한 연구가 이루어지고 있다. 식품 공학이나 의학 분야에서도 유리 상을 나타내는 재료들에 대한 이해와 응용이 중요한 이슈로 떠오르고 있다. 지질학에서는 압력과 조성, 온도에 따른 지각 재료의 유리 상전이 과정이 매우 중요하다. 예를 들어 화산의 분화와 관련해 화구 내 마그마의 유동성, 즉 해당 마그마 조성과 주위 환경에 의해 마그마가 유리 상전이 온도 위에 놓여 있는지 등을 이해하는 것이 화산 분출 메커니즘의 이해에 있어 필수적인 부분이다.
수동적인 입장에서 다른 부분을 보호하거나 빛의 투과만을 담당하는 전통적인 유리의 역할에서 벗어나 능동적 역할을 담당하는 스마트 유리들도 속속 등장하고 있다. 적당한 전압을 가함에 따라 색이나 투과도가 변하는 유리, 기능성 코팅을 통해 스스로 표면을 청소할 수 있는 유리 등이 대표적인 예다. 과학자와 공학자들이 꿈꾸는 미래의 스마트 유리는 낮에는 투명 태양전지로 에너지를 모으고 이를 투명 배터리에 저장한 후 밤에는 디스플레이나 조명으로 변하는 만능 유리다. 반세기 전에 꿈꾸었던 많은 신기술의 상당수가 현실화된 오늘날, 우리가 꿈꾸는 이런 스마트 유리가 가까운 미래에는 일상 속 모습이 될지 어찌 알겠는가?
끝나지 않은 여행
수천 년 동안 사용해 온 유리, 그리고 유리를 다루는 기법은 오늘날 문명을 뒷받침하는 중요한 기반 중 하나다. 그것은 우리의 일상생활에서 유리가 사라진다면, 즉 유리창이 없고 각종 디스플레이의 화면이 사라지고 조명등이 없는 생활을 상상해 본다면 쉽게 알 수 있을 것이다. 따지고 보면 새로운 과학적 발견과 기술적 혁신의 배후에는 대부분 유리라는 물질이 있었다. 유리로 만든 프리즘이 뉴턴의 실험을 통해 빛에 대한 우리의 이해를 깊게 만들었고 지상 위 장난감이었던 망원경 속 렌즈가 갈릴레오의 손에 의해 천상을 향하던 순간 우주에 대한 아리스토텔레스의 세계관이 무너졌다. 근대 화학의 아버지라 불리는 라부아지에의 손에도, 독일 유리 산업을 이끌며 태양 스펙트럼의 흡수선을 발견했던 프라운호퍼의 손에도 유리로 만든 도구들이 들려 있었다. 현대 기술 문명에서 유리가 차지하는 중요성을 기념해서 지난 5월 열린 유엔총회에선 2022년을 ‘국제 유리의 해International Year of Glass’로 선포한 바 있다.[15]
이처럼 우리는 유리를 온갖 분야에 응용하고 자유자재로 활용해 왔고, 유리의 활용성을 더욱 높여가고 있지만 유리가 왜 유리가 되어야 하는지, 그 미시적 정체는 무엇인지에 대해선 아직 합의된 이론이 없다. 앤더슨이 1995년에 유리 상전이 문제의 중요성을 제기한 후[16], 미국에서 발행하는 잡지 <사이언스>가 2005년에 125주년 기념을 맞아 과학계의 각 분야별로 우리가 아직 이해하지 못하고 있는 문제들을 집대성해 보도했다. 질문 중 하나는 “유리상의 본질은 무엇인가?”였다. 이에 대한 이론적, 실험적 모색이 백가쟁명 식으로 진행되면서 하버드 물리학과 데이비드 와이츠David A. Weitz 교수는 다음과 같은 농담을 던진 바 있다.[17]
“유리에 대한 이론을 제안한 이론가들의 수보다 유리 상전이에 대한 이론이 더 많다.”
“There are more theories of the glass transition than there are theorists who propose them.“
어쩌면 우린 21세기가 끝나는 시점에 그에 대한 질문을 다시 던져야 할 수도 있다. 우리에게 가장 친숙한 산화물 유리에서 보이는 구조적, 동적 특성들은 고분자 유리나 스핀 유리를 포함, 매우 다양한 유리 상전이 물질들에서 보편적으로 발견되어 왔지만 유리와 직접 관련짓기 힘든 계에서도 유리의 특성이 관찰되면서 연구의 대상은 점점 더 확대되어 왔다. 콜로이드 유리, 박테리아나 개미 군집 등의 생물학적 기제에서 발생하는 유리 현상이 몇 가지 예다. 결국 유리의 연구의 종착점은 유리의 동역학을 보이는 이런 천태만상의 다양한 계에 적용할 수 있는 보편적 이론을 확립하는 것이다. 과학자들은 점점 더 많은 실험적 증거를 축적해 가고 있고 이를 보편화, 일반화해 있으며 컴퓨터 전산모사를 동원한 이론적 접근도 더 정교하고 치밀해지고 있다. 그 과정에서 유리 이론은 새로운 분야로 전파되어 학문적 기여를 하기도 한다. 예를 들어 자성체 분야에서 매우 방대한 이론적 체계를 구축했던 스핀 유리는 네트워크나 정보 이론을 포함한 새로운 분야의 기반이 되었다.
이번 글의 서두에서 얘기했던 일화는 유리의 응용과 유리 본성에 대한 연구는 사실상 별개로 진행되어 온 측면이 있다는 점을 시사했다. 유리의 응용이 다분히 수천 년 동안 축적되어 온 경험에 기댄 측면이 큰 반면에 과학적 연구의 대상으로서 유리는 그 복잡성으로 인해 지금도 많은 과학자들을 괴롭히고 있다. 그리고 그 연구의 결과물은 신경망을 포함한 엉뚱한 분야의 과학적 진전을 이끌어 왔다. 유리에 대한 과학자들의 이해가 이번 세기말에는 어디까지 가 닿을지 누구도 예측하지 못하겠지만, 그리고 비록 유리 상전이에 대한 완벽한 설명에는 이르지 못한다 하더라도, 그 연구의 끝에는 새로운 물리와 새로운 이론, 그리고 새로운 기술적 혁신이 기다리고 있음은 분명할 것이다.
유리 연구 만세! 국제 유리의 해 만세!!
참고문헌
- J. Langer, “The mysterious glass transition”, Physics Today 60, 8 (2007).
- L. Berthier 외, “Facets of glass physics”, Physics Today 69, 40 (2016).
- Natalie Wolchover, "Ideal Glass Would Explain Why Glass Exists at All" , Quantamagazine, 2020.03.11.
- T. Hecksher 외, “Little evidence for dynamic divergences in ultraviscous molecular liquids”, Nature Physics 4, 737 (2008).
- J. C. Martinez-Garcia 외, “Divergent dynamics and the Kauzmann temperature in glass forming systems”, Scientific Reports 4, 5160 (2014).
- Binder 외, “Spin glasses: Experimental facts, theoretical concepts, and open questions”, Reviews of Modern Physics 58, 801(1986).
- Khomenko 외, “Depletion of Two-Level Systems in Ultrastable Computer-Generated Glasses”, Physical Review Letters 124, 225901 (2020).
- Zhao 외, “Using 20-million-year-old amber to test the super-Arrhenius behaviour of glass-forming systems”, Nature Communications 4, 1783 (2012).
- S. F. Swallen 외, “Organic glasses with exceptional thermodynamic and kinetic stability”, Science 315, 353 (2007).
- T. Pérez-Castañeda 외, “Suppression of tunneling two-level systems in ultrastable glasses of indomethacin”, PNAS 111, 11275 (2014).
- T. Pérez-Castañeda 외, “Two-Level Systems and Boson Peak Remain Stable in 110-Million-Year-Old Amber Glass”, Physical Review Letters 112, 165901 (2014).
- F. Kotz 외, “Three-dimensional printing of transparent fused silica glass”, Nature 544, 337 (2017).
- L. Pegg, “Turning nuclear waste into glass”, Physics Today, 68, 33 (2015).
- J. Schroers, “Bulk metallic glasses”, Physics Today, 66, 32 (2013).
- Internaional Year of Glass, Homepage
- P. W. Anderson, Science 267, 1615 (1995).
- "Anything but clear" , The New York Times, 2008.07.29.